I mattoni o i composti che i peptidi e le proteine del trucco sono aminoacidi.
La molecola di aminoacidi è costituita da un gruppo amminico e un gruppo carbossilico legato a un carbonio tetraedrico. Questo carbonio è noto come -carbonio (alfa -carbonio).
A parte le loro catene laterali, gli aminoacidi possono anche essere distinti dai loro gruppi R. Ci saranno differenze nella struttura, nella carica elettrica e nella polarità di ciascun gruppo di aminoacidi R.
Se sei interessato a un elenco degli aminoacidi più pesanti a leggeri, rimanete sintonizzati su questo pezzo per saperne di più:
1. triptofano
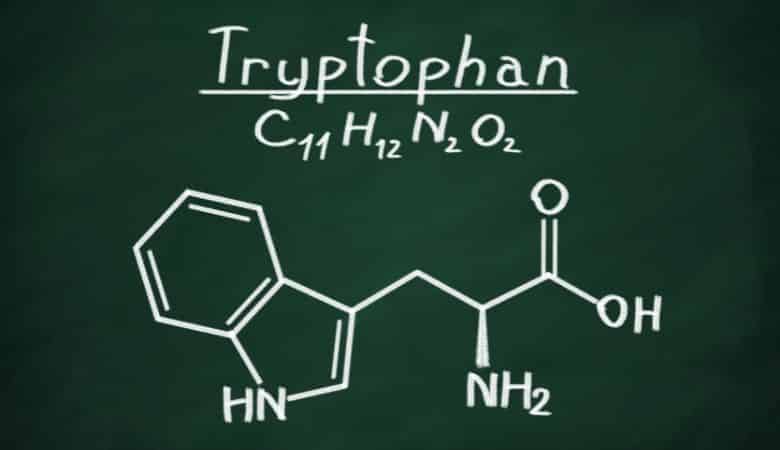
Il triptofano (simbolo TRP o W) è un -aminoacido richiesto per la sintesi proteica. In particolare, il triptofano contiene tre gruppi di aminoacidi: un gruppo amminico, un gruppo di acido carbossilico e un indolo a catena laterale, rendendolo un aminoacido aromatico non polare. Di conseguenza, non può essere sintetizzato dal corpo e deve essere ottenuto dal cibo.
Inoltre, il triptofano è un precursore di serotonina, melatonina e vitamina B3. È codificato dal codone UGG. In cima alla lista degli aminoacidi più pesanti con un peso molecolare di 204,23.
2. Tirosina
L'amminoacido L-tirosina o tirosina (simbolo y o Tyr) è uno dei 20 aminoacidi utilizzati nella sintesi proteica dalle cellule. L'amminoacido ha gruppi laterali polari, rendendolo non essenziale.
La tirosina prende il nome dalla parola greca per il formaggio, il tiro, come fu scoperto nella caseina di formaggio nel 1846 dal chimico tedesco Justus von Liebig.
Nel contesto di un gruppo funzionale o della catena laterale, viene definito tirosile. Nonostante la sua classificazione idrofobica, la tirosina è più idrofila della fenilalanina.
Un RNA messaggero contiene i codoni UAA e UAU che codificano questa proteina. La tirosina è uno degli aminoacidi più pesanti con un peso molecolare di 181,19.
3. Arginina
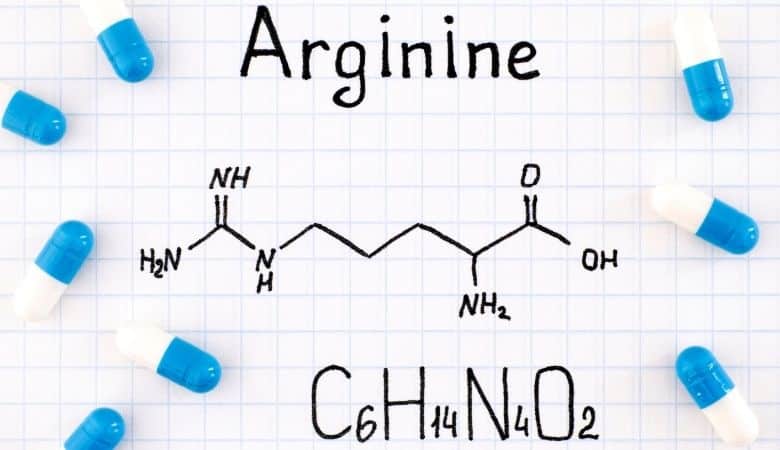
L'aminoacido arginina, noto anche come L-arginina (simbolo Arg o R), viene utilizzato dal corpo per sintetizzare le proteine. Questo composto è costituito da un gruppo amminico, un gruppo di acido carbossilico e una catena laterale che è una catena di dritta alifatica con tre carboni che terminano in guanidine.
L'arginina è un aminoacido alifatico caricato dopo la protonazione dell'acido carbossilico (*COO*), la protonazione del gruppo amminico (*NH3) e la protonazione del gruppo Guanidino (-C- (NH2) 2). È il precursore della biosintesi dell'ossido nitrico. Questo gene è codificato dai codoni CGU, CGC, CGA, CGG, AGA e AGG.
Gli aminoacidi semi essenziali e condizionalmente essenziali possono essere derivati dall'arginina, a seconda della fase di sviluppo individuale e dello stato di salute. Passa anche come uno degli aminoacidi più pesanti con un peso molecolare di 174,20.
4. istidina
L'amminoacido istidina (simbolo suo o H) è essenziale per la sintesi proteica.
È composto da tre gruppi amminici (che sono protonati in condizioni fisiologiche -NH3 e gruppi di acido carbossilico che sono deprotonati in condizioni fisiologiche -coo*) e una catena laterale di imidazolo (che è parzialmente protonato), rendendolo un aminoacido caricato positivamente sotto condizioni fisiologiche.
In studi recenti, è stato dimostrato di essere essenziale anche per gli adulti, nonostante sia inizialmente ritenuto essenziale solo nei bambini.
I codoni Cau e CAC sono responsabili della sua codifica. L'istidina è uno degli aminoacidi più pesanti con un peso molecolare di 155,16.
5. Serina
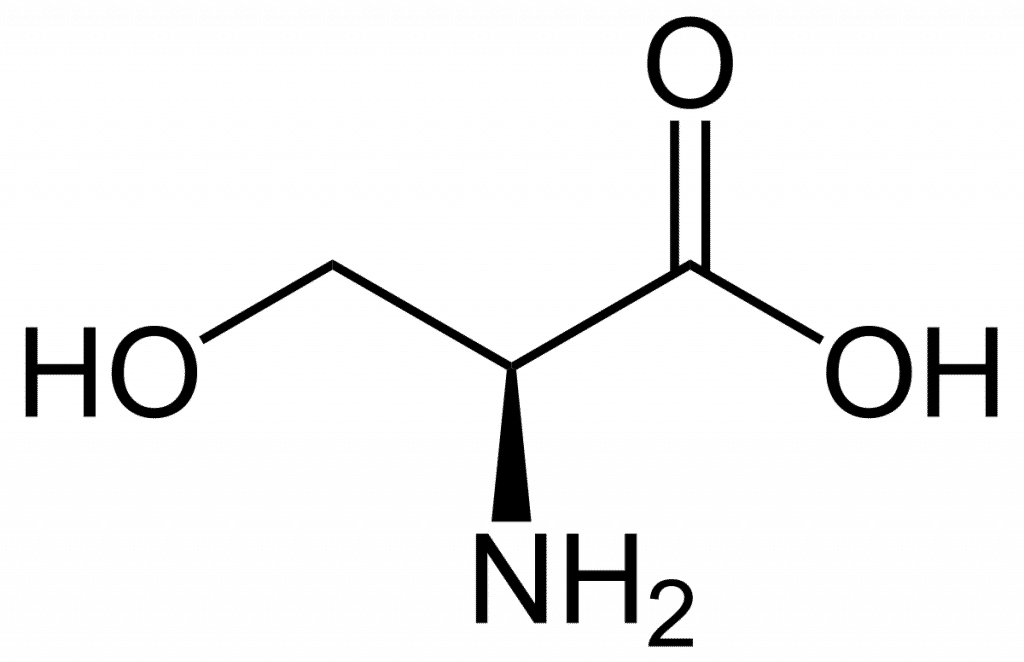
Nella biosintesi delle proteine, la serina (simbolo Ser o S) è un aminoacido essenziale. È costituito da un gruppo amminico (che è protonato nell'ambiente biologico), un gruppo carbossilico (che è deprotonato in condizioni biologiche) e una catena laterale costituita da un gruppo idrossimetile, quindi la sua classificazione come aminoacido polare.
Poiché può essere sintetizzato nel corpo umano in normali condizioni fisiologiche, non è essenziale. Ci sono sei codoni che lo codificano: UCU, UCC, UCA, UCG, AGU e AGC. La serina è uno degli aminoacidi più leggeri con un peso molecolare di 105,9.
6. Alanina
L'aminoacido alanina (simbolo Ala o A) partecipa alla produzione di proteine. L'atomo di carbonio centrale trasporta sia un gruppo di ammina che un gruppo di acido carbossilico attaccato alla sua catena laterale, che è un gruppo metilico.
Di conseguenza, il suo nome sistematico IUPAC è acido 2 -aminopropanoico ed è classificato come un aminoacido alifatico, non polare. In condizioni biologiche, queste molecole esistono nella loro forma zwitterionica, in cui il gruppo di ammina protona (come *NH3) e il gruppo carbossilico si deprotona (come CO2).
Non è essenziale per l'uomo in quanto può essere sintetizzato metabolicamente e non deve essere consumato. I codoni GC (GCU, GCC, GCA e GCG) lo codificano. L'ialanina è uno degli aminoacidi più leggeri con un peso molecolare di 89,10.
7. Glicina

La glicina aminoacida (simbolo gly o g) ha un atomo di idrogeno come catena laterale. Ha la formula chimica NH2CH2COOH, che è l'amminoacido più semplice (l'acido carbamico è instabile).
La glicina è un aminoacido proteinogeno. Tutti i codoni che iniziano con GG codificano (GGU, GGC, GGA, GGG). Per la sua forma compatta, la glicina è essenziale per la formazione di eliche alfa nelle strutture proteiche secondarie.
A causa della sua abbondanza, costituisce anche la maggior parte delle eliche triple di collagene. La glucina è anche un neurotrasmettitore inibitorio, quindi bloccando il suo rilascio all'interno del midollo spinale (come durante un'infezione con clostridium tetani) può portare a paralisi spastica causata da contrazioni muscolari disinibite.
La glicina è l'amminoacido più leggero esistente con un peso molecolare di 75,07.
