Les blocs de construction ou les composés qui maquillent les peptides et les protéines sont des acides aminés.
La molécule d'acide aminé se compose d'un groupe amino et d'un groupe carboxyle lié à un carbone tétraédrique. Ce carbone est connu sous le nom de carbone (alpha-carbone).
Mis à part leurs chaînes latérales, les acides aminés peuvent également être distingués par leurs groupes R. Il y aura des différences dans la structure, la charge électrique et la polarité de chaque groupe Amino Acides R.
Si vous êtes intéressé par une liste des acides aminés les plus lourds aux plus légers, restez à l'écoute de cette pièce pour en savoir plus:
1. tryptophane
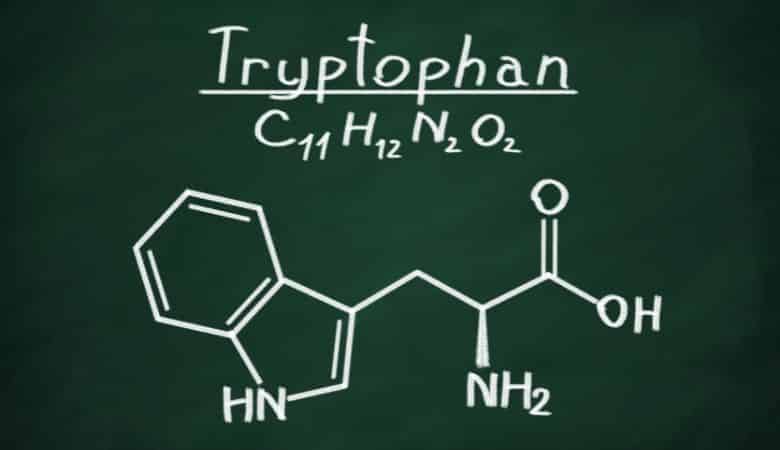
Le tryptophane (symbole TRP ou W) est un-acide aminé requis pour la synthèse des protéines. Plus précisément, le tryptophane contient trois groupes d'acides aminés: un groupe amino, un groupe d'acide carboxylique et un indole de chaîne latérale, ce qui en fait un acide aminé aromatique non polaire. En conséquence, il ne peut pas être synthétisé par le corps et doit être obtenu à partir de nourriture.
De plus, le tryptophane est un précurseur de la sérotonine, de la mélatonine et de la vitamine B3. Il est codé par le codon UGG. Il arrive en tête de la liste des acides aminés les plus lourds avec un poids moléculaire de 204,23.
2. Tyrosine
La L-tyrosine ou la tyrosine de l'acide aminé (symbole Y ou Tyr) est l'un des 20 acides aminés utilisés dans la synthèse des protéines par les cellules. L'acide aminé a des groupes latéraux polaires, ce qui le rend non essentiel.
Tyrosine est nommée d'après le mot grec pour le fromage, Tyro, comme il a été découvert dans le fromage caséine en 1846 par le chimiste allemand Justus von Liebig.
Dans le contexte d'un groupe fonctionnel ou d'une chaîne latérale, il est appelé tyrosyl. Malgré sa classification hydrophobe, la tyrosine est plus hydrophile que la phénylalanine.
Un ARN messager contient les codons UAA et UAU qui codent cette protéine. La tyrosine est l'un des acides aminés les plus lourds avec un poids moléculaire de 181,19.
3. Arginine
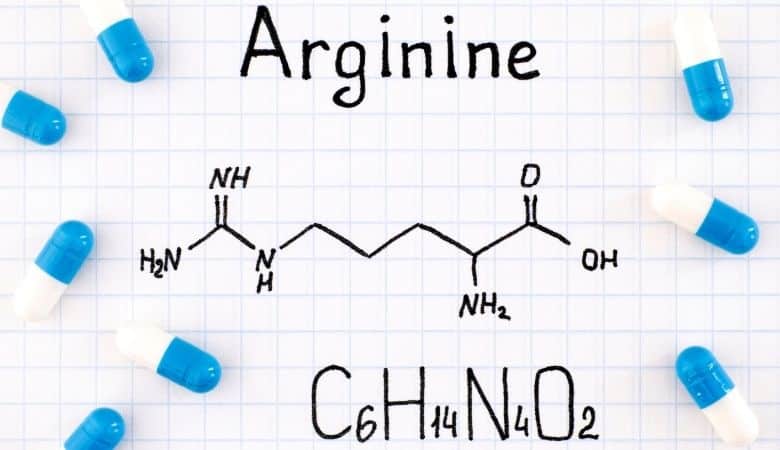
L'arginine d'acide aminé, également connu sous le nom de L-arginine (symbole Arg ou R), est utilisée par le corps pour synthétiser les protéines. Ce composé se compose d'un groupe amino, d'un groupe d'acide carboxylique et d'une chaîne latérale qui est une chaîne droite aliphatique avec trois carbones se terminant par des guanidines.
L'arginine est un acide aminé aliphatique chargé après la protonation de l'acide carboxylique (* COO *), la protonation du groupe amino (* NH3) et la protonation du groupe Guanidino (-C- (NH2) 2). C'est le précurseur de la biosynthèse de l'oxyde nitrique. Ce gène est codé par les codons CGU, CGC, CGA, CGG, AGA et AGG.
Les acides aminés semi-essentiels et conditionnellement essentiels peuvent être dérivés de l'arginine, selon un stade de développement des individus et l'état de santé. Il passe également comme l'un des acides aminés les plus lourds avec un poids moléculaire de 174,20.
4. Histidine
L'histidine d'acide aminé (symbole His ou H) est essentielle pour la synthèse des protéines.
Il est composé de trois groupes amino (qui sont protonés dans des conditions physiologiques -NH3 et des groupes d'acides carboxyliques qui sont déprotonés dans des conditions physiologiques -coo *) et une chaîne latérale d'imidazole (qui est partiellement protonée), ce qui en fait un acide aminé chargé positivement sous conditions physiologiques.
Dans les études récentes, il s'est également avéré essentiel pour les adultes, bien qu'il ne soit considéré comme essentiel que chez les nourrissons.
Les codons CAU et CAC sont responsables de son codage. L'histidine est l'un des acides aminés les plus lourds avec un poids moléculaire de 155,16.
5. Sérine
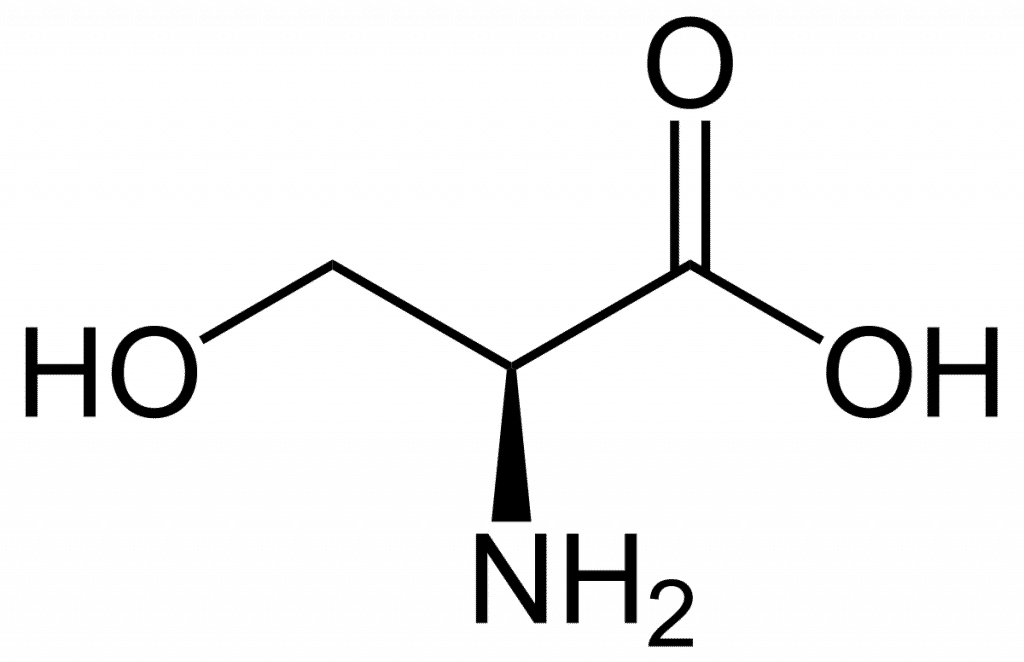
Dans la biosynthèse des protéines, la sérine (symbole Ser ou S) est un acide aminé essentiel. Il se compose d'un groupe amino (qui est protoné dans l'environnement biologique), d'un groupe carboxyle (qui est déprotoné dans des conditions biologiques), et d'une chaîne latérale composée d'un groupe hydroxyméthyle, d'où sa classification comme acide aminé polaire.
Puisqu'il peut être synthétisé dans le corps humain dans des conditions physiologiques normales, il n'est pas essentiel. Il y a six codons qui le codaient: UCU, UCC, UCA, UCG, AGU et AGC. La sérine est l'un des acides aminés les plus légers avec un poids moléculaire de 105,9.
6. Alanine
L'alanine d'acide aminé (symbole ALA ou A) participe à la production de protéines. L'atome de carbone central transporte à la fois un groupe amine et un groupe d'acide carboxylique attaché à sa chaîne latérale, qui est un groupe méthyle.
En conséquence, son nom systématique IUPAC est l'acide 2-aminopropanoïque, et il est classé comme un acide aminé-aminé aliphatique non polaire. Dans des conditions biologiques, ces molécules existent dans leur forme zwitterionique, dans laquelle le groupe amine protona (comme * NH3) et le groupe carboxyle déprotonnent (comme CO2).
Il n'est pas essentiel pour les humains car il peut être synthétisé métaboliquement et n'a pas besoin d'être consommé. Les codons GC (GCU, GCC, GCA et GCG) le codent. L'alanine est l'un des acides aminés les plus légers avec un poids moléculaire de 89.10.
7. Glycine

La glycine à l'acide aminé (symbole Gly ou G) a un atome d'hydrogène comme chaîne latérale. Il a la formule chimique NH2CH2COOH, qui est l'acide aminé le plus simple (l'acide carbamique est instable).
La glycine est un acide aminé protéinogène. Tous les codons qui commencent par GG le codent (GGU, GGC, GGA, GGG). En raison de sa forme compacte, la glycine est essentielle pour la formation d'hélices alpha dans les structures de protéines secondaires.
En raison de son abondance, il constitue également la plupart des triples hélices de collagène. La glucine est également un neurotransmetteur inhibiteur, donc bloquer sa libération dans la moelle épinière (comme lors d'une infection par Clostridium tetani) peut entraîner une paralysie spastique causée par des contractions musculaires non inhibées.
La glycine est l'acide aminé le plus léger qui existe avec un poids moléculaire de 75,07.
