Celtniecības bloki vai savienojumi, kas aplauzuma peptīdi un olbaltumvielas ir aminoskābes.
Aminoskābes molekula sastāv no amino grupas un karboksilgrupas, kas piesaistīta tetraedriskajam ogleklim. Šis ogleklis ir pazīstams kā -ogleklis (alfa -ogleklis).
Papildus viņu sānu ķēdēm aminoskābes var atšķirt arī ar viņu R grupām. Katras aminoskābju R grupas struktūrā, elektriskajā lādiņā un polaritātē būs atšķirības.
Ja jūs interesē visvieglākās aminoskābju smagāko vai visvieglāko sarakstu, sekojiet līdzi šim skaņdarbam, lai uzzinātu vairāk:
1. Tryptophan
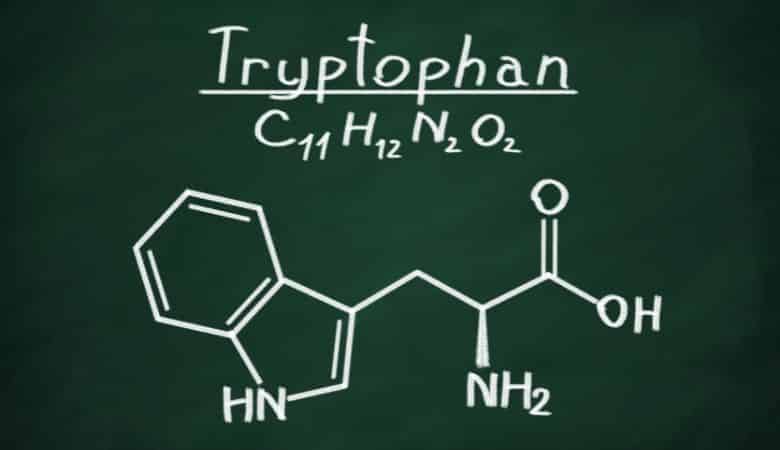
Tryptophan (simbols TRP vai W) ir -aminskābe, kas nepieciešama olbaltumvielu sintēzei. Konkrēti, triptofāns satur trīs aminoskābju grupas: aminogrupu, karbonskābes grupu un sānu ķēdi indolu, padarot to par nepolāru aromātisku aminoskābi. Rezultātā to nevar sintezēt ķermenis, un tas jāiegūst no pārtikas.
Turklāt triptofāns ir serotonīna, melatonīna un B3 vitamīna priekšgājējs. To kodē UGG kodons. Tas papildina smagāko aminoskābju sarakstu ar molekulmasu 204,23.
2. Tirozīns
Aminoskābes L-tirozīns vai tirozīns (simbols y vai tyr) ir viena no 20 aminoskābēm, ko šūnas izmanto olbaltumvielu sintēzē. Aminoskābei ir polārās sānu grupas, padarot to nebūtisku.
Tirozīns ir nosaukts pēc grieķu vārda sieram, tiro, kā to 1846. gadā atklāja siera kazeīnā vācu ķīmiķis Justus fon Liebig.
Funkcionālās grupas vai sānu ķēdes kontekstā to sauc par tirozilu. Neskatoties uz hidrofobisko klasifikāciju, tirozīns ir hidrofīlāks nekā fenilalanīns.
Messenger RNS satur kodonus UAA un UAU, kas kodē šo olbaltumvielu. Tirozīns ir viena no smagākajām aminoskābēm ar molekulmasu 181,19.
3. Arginīns
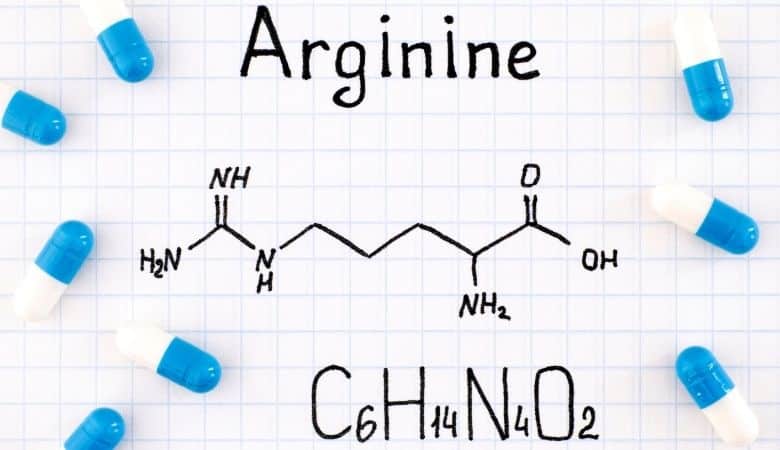
Aminoskābes arginīnu, kas pazīstams arī kā l-arginīns (simbols arg vai r), ķermenis izmanto olbaltumvielu sintezēšanai. Šis savienojums sastāv no amino grupas, karbonskābes grupas un sānu ķēdes, kas ir alifātiska taisna ķēde ar trim oglekļiem, kas beidzas ar guanidīniem.
Arginīns ir uzlādēta alifātiska aminoskābe pēc karbonskābes (*COO*) protonēšanas, aminogrupas protonēšana (*NH3) un Guanidino grupas protonēšana (-c- (NH2) 2). Tas ir slāpekļa oksīda biosintēzes priekšgājējs. Šo gēnu kodē Codons CGU, CGC, CGA, CGG, AGA un AGG.
Daļēji būtiskas un nosacītas būtiskas aminoskābes var iegūt no arginīna, atkarībā no indivīdu attīstības stadijas un veselības stāvokļa. Tas arī iet kā viena no smagākajām aminoskābēm ar molekulmasu 174,20.
4. Histidīns
Aminoskābes histidīns (simbols viņa vai h) ir būtisks olbaltumvielu sintēzei.
Tas sastāv no trim aminogrupām (kuras protonē fizioloģiskos apstākļos -NH3 un karbonskābes grupas, kuras fizioloģiskos apstākļos ir deprotonētas -coo*) un viena imidazola sānu ķēde (kas daļēji tiek protonēta), padarot to par pozitīvi uzlādētu aminoskābi zem tā zem aminoskābes zem aminoskābes zem aminoskābes zem aminoskābes Fizioloģiskie apstākļi.
Jaunākajos pētījumos ir pierādīts, ka tas ir būtisks arī pieaugušajiem, neskatoties uz to, ka sākotnēji tika uzskatīts, ka tas ir būtisks tikai zīdaiņiem.
Kodoni Cau un CAC ir atbildīgi par tā kodēšanu. Histidīns ir viena no smagākajām aminoskābēm ar molekulmasu 155,16.
5. serīns
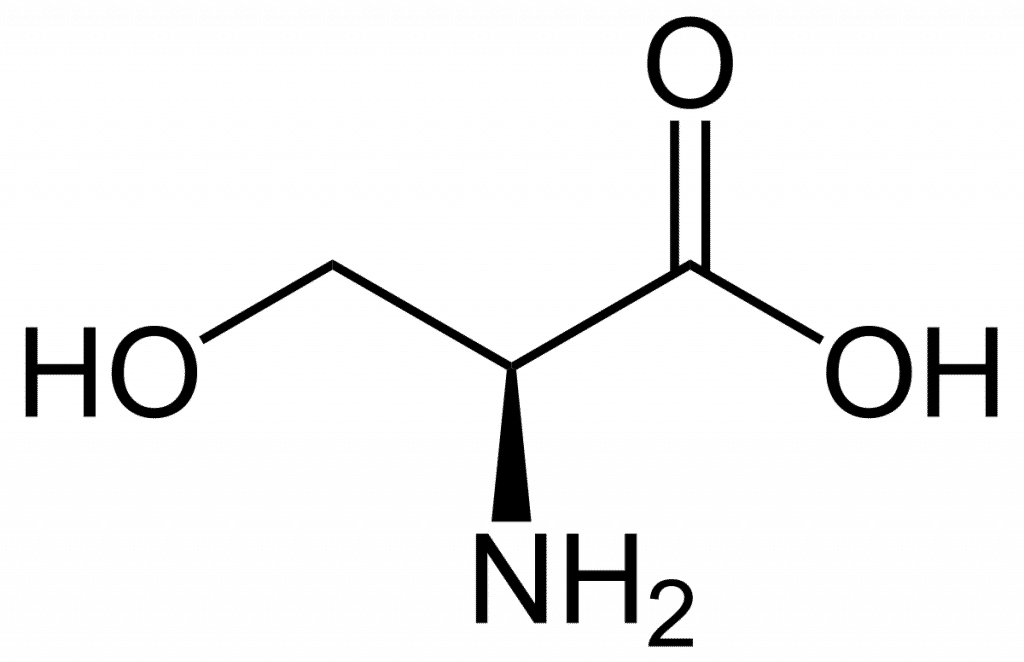
Olbaltumvielu biosintēzē serīns (simbols SER vai S) ir neaizstājama aminoskābe. Tas sastāv no amino grupas (kas ir protonēta bioloģiskajā vidē), karboksilgrupa (kas bioloģiskos apstākļos tiek deeprotonēta), un sānu ķēdi, kas sastāv no hidroksimetilgrupas, līdz ar to tā klasificē kā polāro aminoskābi.
Tā kā to var sintezēt cilvēka ķermenī normālos fizioloģiskos apstākļos, tas nav būtisks. Ir seši kodoni, kas to kodē: UCU, UCC, UCA, UCG, AGU un AGC. Serīns ir viena no vieglākajām aminoskābēm ar molekulmasu 105,9.
6. Alanīns
Aminoskābes alanīns (simbols ALA vai A) piedalās olbaltumvielu ražošanā. Centrālajam oglekļa atomam ir gan amīnu grupa, gan karbonskābes grupa, kas piestiprināta pie tās sānu ķēdes, kas ir metilgrupa.
Rezultātā tā IUPAC sistemātiskais nosaukums ir 2 -aminopropānskābe, un to klasificē kā alifātisku, nepolāru -aminoskābi. Bioloģiskos apstākļos šīs molekulas pastāv to cwitterionic formā, kuros amīnu grupas protonāti (kā *NH3) un karboksilgrupa deprotonāti (kā CO2).
Tas nav svarīgi cilvēkiem, jo to var sintezēt metaboliski un nav jālieto. GC kodoni (GCU, GCC, GCA un GCG) to kodē. Alanīns ir viena no vieglākajām aminoskābēm ar molekulmasu 89,10.
7. glicīns

Aminoskābes glicīnam (simbolam Gly vai G) ir viens ūdeņraža atoms kā sānu ķēde. Tam ir ķīmiskā formula NH2CH2COOH, kas ir vienkāršākā aminoskābe (karbamīnskābe ir nestabila).
Glicīns ir proteinogēna aminoskābe. Visi kodoni, kas sākas ar GG, to kodē (GGU, GGC, GGA, GGG). Sakarā ar kompakto formu glicīns ir būtisks alfa spirāles veidošanai sekundārajā olbaltumvielu struktūrās.
Tā kā tā ir pārpilnība, tas arī veido lielāko daļu kolagēna trīskāršo helice. Glikīns ir arī inhibējošs neirotransmiters, tāpēc tā izdalīšanās bloķēšana muguras smadzenēs (piemēram, infekcijas laikā ar Clostridium tetani) var izraisīt spastisku paralīzi, ko izraisa neiesaistītas muskuļu kontrakcijas.
Glicīns ir vieglākā aminoskābe, kas pastāv ar molekulmasu 75,07.
